Giới thiệu
Trong học tập và nghiên cứu, việc tính toán một cách chính xác phần trăm khối lượng của các nguyên tố và hợp chất là rất quan trọng. Phần trăm khối lượng không chỉ giúp chúng ta hiểu rõ hơn về thành phần của một chất mà còn hỗ trợ trong nhiều lĩnh vực khác nhau như hóa học, sinh học, và khoa học vật liệu. Ngày hôm nay, chúng ta sẽ tìm hiểu về cách thức thực hiện việc này một cách đơn giản và hiệu quả.
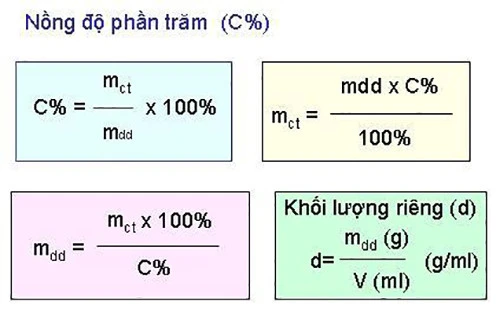
Cơ sở lý thuyết về phần trăm khối lượng
1. Định nghĩa phần trăm khối lượng
Phần trăm khối lượng của một nguyên tố trong hợp chất được tính bằng công thức:
\[ \text{Phần trăm khối lượng} (\%) = \left( \frac{\text{Khối lượng mol của nguyên tố}}{\text{Khối lượng phân tử của hợp chất}} \right) \times 100 \]
Khối lượng mol của nguyên tố là khối lượng của một mol nguyên tử của nguyên tố đó, trong khi khối lượng phân tử là tổng khối lượng của tất cả các nguyên tử trong một phân tử của hợp chất.
2. Ý nghĩa của phần trăm khối lượng
Phần trăm khối lượng cung cấp thông tin về tỉ lệ của một nguyên tố cụ thể trong toàn bộ hợp chất. Điều này có giá trị trong nhiều trường hợp, chẳng hạn như:
- Giúp xác định tính chất hóa học của hợp chất.
- Hỗ trợ trong việc dự đoán hành vi của hợp chất trong các phản ứng hóa học.
- Hữu ích trong việc tính toán lượng nguyên liệu cần thiết cho các phản ứng hóa học.
Các bước tính toán phần trăm khối lượng
1. Xác định công thức hóa học của hợp chất
Trước hết, bạn cần biết công thức hóa học của hợp chất mà bạn muốn tính toán. Ví dụ, đối với hợp chất nước (H₂O), công thức hóa học cho thấy có 2 nguyên tử hydro và 1 nguyên tử oxy.
2. Tính khối lượng mol của các nguyên tố
Tiếp theo, bạn cần tra cứu khối lượng mol của các nguyên tố trong bảng tuần hoàn. Đối với ví dụ trên:
- Khối lượng mol của hydro (H) là khoảng 1 g/mol.
- Khối lượng mol của oxy (O) là khoảng 16 g/mol.
3. Tính khối lượng phân tử của hợp chất
Khối lượng phân tử được tính bằng cách cộng khối lượng mol của tất cả các nguyên tố trong hợp chất. Đối với nước, khối lượng phân tử sẽ là:
\[ \text{Khối lượng phân tử của H₂O} = (2 \times 1) + 16 = 18 \text{ g/mol} \]
4. Tính phần trăm khối lượng
Áp dụng công thức trên để tính phần trăm khối lượng của mỗi nguyên tố:
- Phần trăm khối lượng của H là:
\[ \text{Phần trăm khối lượng của H} = \left( \frac{2 \times 1}{18} \right) \times 100 \approx 11.11\% \]
- Phần trăm khối lượng của O là:
\[ \text{Phần trăm khối lượng của O} = \left( \frac{16}{18} \right) \times 100 \approx 88.89\% \]

Ví dụ chi tiết về tính phần trăm khối lượng
Hãy cùng xem xét một ví dụ cụ thể khác để hiểu rõ hơn về cách tính phần trăm khối lượng trong một hợp chất phức tạp hơn. Giả sử chúng ta muốn tính phần trăm khối lượng của các nguyên tố trong hợp chất Calcium Sulfate (CaSO₄).
1. Tính khối lượng mol của các nguyên tố
- Khối lượng mol của calcium (Ca) là khoảng 40 g/mol.
- Khối lượng mol của sulfur (S) là khoảng 32 g/mol.
- Khối lượng mol của oxygen (O) là khoảng 16 g/mol, nhưng vì có 4 nguyên tử oxy, ta sẽ tính là 4 × 16 = 64 g/mol.
2. Tính khối lượng phân tử của hợp chất CaSO₄
Khối lượng phân tử sẽ là:
\[ \text{Khối lượng phân tử của CaSO₄} = 40 + 32 + 64 = 136 \text{ g/mol} \]
3. Tính phần trăm khối lượng
- Phần trăm khối lượng của Ca là:
\[ \text{Phần trăm khối lượng của Ca} = \left( \frac{40}{136} \right) \times 100 \approx 29.41\% \]
- Phần trăm khối lượng của S là:
\[ \text{Phần trăm khối lượng của S} = \left( \frac{32}{136} \right) \times 100 \approx 23.53\% \]
- Phần trăm khối lượng của O là:
\[ \text{Phần trăm khối lượng của O} = \left( \frac{64}{136} \right) \times 100 \approx 47.06\% \]

Những lưu ý khi tính toán
1. Độ chính xác của số liệu
Khi tính phần trăm khối lượng, điều quan trọng là phải sử dụng các giá trị khối lượng mol chính xác từ bảng tuần hoàn, vì sai sót nhỏ có thể dẫn đến kết quả không chính xác.
2. Kiểm tra lại các phép tính
Trước khi đưa ra kết quả cuối cùng, bạn nên kiểm tra lại từng bước tính toán để đảm bảo không có sai sót nào trong các phép cộng, nhân hay chia.
3. Ứng dụng thực tế
Phần trăm khối lượng có thể được ứng dụng trong nhiều lĩnh vực như kiểm tra chất lượng sản phẩm trong ngành công nghiệp thực phẩm, xác định thành phần hóa học trong các nghiên cứu khoa học, và nhiều ứng dụng khác trong đời sống hàng ngày.
Kết luận
Tính toán phần trăm khối lượng là một kỹ năng hữu ích và cần thiết trong nhiều lĩnh vực khác nhau. Bằng cách nắm vững quy trình và công thức tính toán, bạn sẽ có thể áp dụng kiến thức này vào các bài tập hóa học cũng như trong thực tiễn. Hy vọng rằng bài viết này đã mang đến cho bạn những thông tin bổ ích và dễ áp dụng. Hãy thực hành thêm với nhiều hợp chất khác nhau để củng cố kiến thức của mình nhé!